
随着流感病毒的再次来袭,许多人开始关注抗流感药物的选择。奥司他韦作为经典的流感治疗药物,已经被广泛应用近20年,凭借其确切的疗效和较高的安全性,深受医生和患者的青睐。然而,近年一款名为玛巴洛沙韦(商品名:速福达?)的药物进入了大众的视野,凭借“只需服用一次”的宣传,它被誉为“流感神药”。但是,玛巴洛沙韦的所谓“奇迹疗效”真的有那么简单和有效吗?药物在体内长时间停留的影响又会带来哪些潜在问题?

1. 为什么只需吃一次?
玛巴洛沙韦是一种前体药物,服用后会在体内通过转化为活性代谢产物——巴洛沙韦,进而发挥抗病毒作用。该药物具有较长的半衰期,活性代谢产物在体内的持续时间超过了流感病毒的潜伏期。因此,玛巴洛沙韦在服用后能保持有效浓度较长时间,理论上只需服用一次即可治疗流感。
根据临床研究,玛巴洛沙韦的半衰期在中国健康成人受试者中为99.7小时(约4.15天),服药后120小时(约5天),血药浓度仍高于有效浓度。这样长的半衰期使得药物能够持续发挥作用,减少了患者服药的频率。
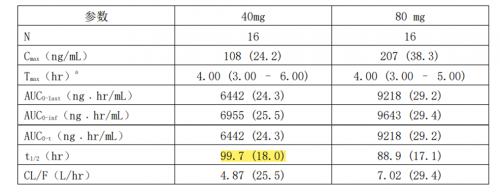
图1:中国健康成人受试者在空腹状态下单次口服40mg或80mg后的药代动力学参数
注:①药物的半衰期(t1/2),血液中药物浓度降低到峰值的一半所用的时间;②流感抗病毒治疗疗程一般为5~7天。
2. 药物在体内长时间停留的隐患
尽管长时间的药物停留为患者提供了服药便利,但这一特点也带来了许多潜在风险。药物在体内长时间滞留,可能会引发以下一系列健康问题。
2.1 服用过量后的难以处理
玛巴洛沙韦的过量使用后果并不明确。由于缺乏已知的特效解毒剂,且活性代谢产物与血清蛋白结合率高达92.9%-93.9%,透析无法有效清除药物残留。一旦发生过量用药,患者只能接受标准支持性治疗,而无法迅速去除体内药物。这意味着,药物过量的后果可能会对患者的健康带来严重的影响,且恢复过程漫长。
2.2 药物过敏反应的持续影响
玛巴洛沙韦可能引发一些过敏反应,包括速发过敏性休克等。对于出现过敏反应的患者,必须持续进行抗过敏治疗,直到药物完全清除出体外。这一过程可能需要20多天,极大地增加了患者的负担和治疗时间。
2.3 与其他药物的相互作用
玛巴洛沙韦在与其他药物的共同使用时,可能会引发不良反应。例如,含有多价阳离子的制剂(如铁、钙、镁等补充剂)会显著降低玛巴洛沙韦的血浆浓度。因此,患者应避免与这些药物同服。此外,玛巴洛沙韦还可能影响流感疫苗的接种效果。根据《中国流感疫苗预防接种技术指南(2023-2024)》的建议,使用过玛巴洛沙韦的患者应推迟接种流感减毒活疫苗。
2.4 哺乳期的风险
虽然玛巴洛沙韦是否会分泌到母乳中尚无明确结论,但已有动物实验显示,药物及其代谢产物可分泌到大鼠的乳汁中药物及其代谢产物可能通过乳汁分泌至哺乳期婴儿体内。因此,服用玛巴洛沙韦的哺乳期妇女应停止哺乳,并且停止哺乳的时间可能需要根据药物在体内的残留时间进一步延长。
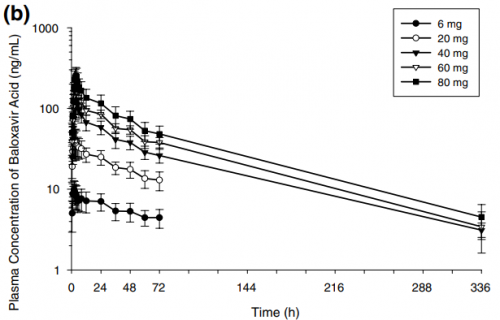
图2:单次口服不同剂量后的血浆药物浓度随时间变化曲线
3. 吃了1次药,流感就完全治愈了吗?
玛巴洛沙韦的一大卖点是“只需吃一次药”,就能治愈流感。但事实上,流感的治疗远没有这么简单。药物的作用主要是缩短病程并缓解症状,而不是立即让症状消失。
3.1 流感治疗需要时间
研究显示,玛巴洛沙韦对流感症状的缓解并非立竿见影。对于既往健康的成人和青少年患者,服药后,平均需要53.7小时才能使症状得到缓解。对于高风险患者,症状缓解的时间则需要更长,达到73.2小时,治疗效果与奥司他韦相当。因此,虽然服用一次药物能有效缓解症状,但并不意味着症状会立即消失,患者仍需耐心等待。
3.2 即使吃了1次药,症状可能会反复
根据日本上市后监测数据,玛巴洛沙韦使用后,一些患者会出现“双相热”,即发热消退后再次发热,尤其是在65岁以上的老年人和6岁以下的儿童中,复发的发生率更高,分别为9.57%和12.5%。因此,服用一次药后,流感症状仍然可能会反复出现,患者需要继续监测病情。
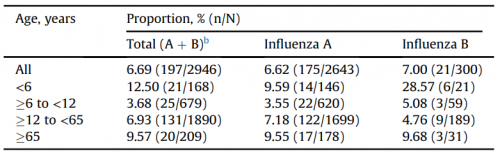
图3:患者双相热发生率(按年龄和流感病毒分类)
理性看待“流感神药”
虽然玛巴洛沙韦因其“一次性服用”的便捷性而备受推崇,但药物在体内长时间停留所带来的副作用和健康风险不容忽视。服药后可能发生的过敏反应、与其他药物的相互作用以及对哺乳期妇女的潜在影响,都要求我们在使用该药时必须谨慎对待。
作为消费者和患者,我们应理性看待这类药物的广告宣传,了解药物的利弊,在医生指导下进行科学用药。流感的治疗应是综合性的,而不仅仅依赖单一药物。我们不仅要关注药物的疗效,更要关注药物使用后的长期影响,避免因不当使用而带来的健康风险。
参考文献:
[1]玛巴洛沙韦片说明书. 修改日期:2023年03月21日.
[2]速福达TM(玛巴洛沙韦片)产品信息介绍.
[3]中国疾控中心. 中国流感疫苗预防接种技术指南(2023-2024).
[4]Koshimichi H, Ishibashi T, Kawaguchi N, et al. Safety, Tolerability, and Pharmacokinetics of the Novel Anti-influenza Agent Baloxavir Marboxil in Healthy Adults: Phase I Study Findings. Clin Drug Investig. 2018;38(12):1189-1196.
[5]Hayden FG, Sugaya N, Hirotsu N, et al. Baloxavir Marboxil for Uncomplicated Influenza in Adults and Adolescents. N Engl J Med. 2018;379(10):913-923.
[6]Ison MG, Portsmouth S, Yoshida Y, et al. Early treatment with baloxavir marboxil in high-risk adolescent and adult outpatients with uncomplicated influenza (CAPSTONE-2): a randomised, placebo-controlled, phase 3 trial. Lancet Infect Dis. 2020;20(10):1204-1214.
[7]Nakazawa M, Hara K, Komeda T, et al. Safety and effectiveness of baloxavir marboxil for the treatment of influenza in Japanese clinical practice: A postmarketing surveillance of more than 3000 patients. J Infect Chemother. 2020;26(7):729-735.
声明:以上内容为本网站转自其它媒体,相关信息仅为传递更多企业信息之目的,不代表本网观点,亦不代表本网站赞同其观点或证实其内容的真实性。投资有风险,需谨慎。

